 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
Cl2/Cl-和Cu2+/Cu的标准电极电势分别是1.36V和0.34V,反应Cu2+(aq)+2Cl-(aq)====Cu(s)+Cl2(g)的标准电动势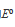 是( )V。
是( )V。
A.-2.38
B.-1.70
C.-1.02
D.+1.70
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
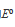 是( )V。
是( )V。A.-2.38
B.-1.70
C.-1.02
D.+1.70
 答案
答案
 更多“Cl2/Cl-和Cu2+/Cu的标准电极电势分别是1.36V和0.34V,反应Cu2+(aq)+2Cl-(aq)====Cu(s)+Cl2(g)的标准电动势是”相关的问题
更多“Cl2/Cl-和Cu2+/Cu的标准电极电势分别是1.36V和0.34V,反应Cu2+(aq)+2Cl-(aq)====Cu(s)+Cl2(g)的标准电动势是”相关的问题
第1题
已知




第2题
求下列反应在298.15K的标准摩尔反应焓变298.15K。
(1)Fe(s)+Cu2+(aq)→Fe2+(aq)+Cu(s)
(2)AgCl(s)+Br-(aq)→AgBr(s)+Cl-(aq)
(3)Fe2O3(s)+6H+(aq)→2Fe3+(aq)+3H2O(l)
(4)Cu2+(aq)+Zn(s)→Cu(s)+Zn2+(aq)
第3题
将铜片插入含l.0 mol.L-1氨水和1.0 mol.L-1[Cu(NH3)4]2+的溶液中构成一个半电池,将此半电池与标准氢电极组成原电池,测得其电动势Eθ=0.030 V,且知标准氢电极在此作正极。试计算[Cu(NH3)4]2+的K稳θ。(已知:Eθ(Cu2+/Cu)=0.337 V)
第4题
已知Eθ(MnO-4/Mn2+)=1.51V,Eθ(Cl2/Cl-)=1.36V,若将此两电对组成原电池,请写出:
(1)该电池的电池符号;
(2)写出正负电极的电极反应和电池反应以及电池标准电动势;
(3)计算电池反应在25℃时和Kθ;
(4)当[H+] = 1.0×10-2mol•L-1,而其他离子浓度均为1.0 mol•L-1,= 100 kPa时的电池电动势.
第5题
B.标准状态下,MnO4-的氧化性比Cl2强,因为在电极反应中MnO4-得到的电子多
C.已知电极反应Cl2+2e-→2Cl-的φθ=1.36V,则电极反应1/2Cl2+e-→Cl-的φθ=0.68V
D.CrO42-和Cr2O72-两离子中Cr的氧化值相等
第6题
A.O32-、Cl-、OH-
B.O32-、OH-、Cl-
C.l-、OH-、CO32-
D.OH-、Cl-、CO32-
第8题
A.l2与H2O反应:Cl2+H2O = 2H++ClO-+ Cl-
B.向Na2SiO3溶液中逐滴加入稀盐酸:2H+ +SiO32- ═ H2SiO3(胶体)
C.向AlCl3溶液中滴加氨水至过量:Al3+ + 3OH- ══ Al(OH)3↓
D.将铜片投入稀盐酸中: Cu + 2H+ = Cu2+ + H2↑
第9题
298K时,在Ag+/Ag电极中加入过量I-,设达到平衡时c(I-)=0.1mol·dm-3,而另一电极为Cu2+/Cu,c(Cu2+)=0.01mol·dm-3,将两电极组成原电池,写出原电池符号、电池反应,并求电池反应平衡常数。
已知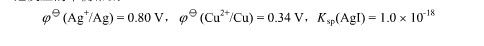
第10题
A.Fe3+和Cu
B.Fe2+和Sn2+
C.Cu2+和Fe
D.Fe3+和Fe