 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知下列100kPa,298K时的热力学数据: (1)试通过热力学计算,说明下面反应298K时的进行方向:
已知下列100kPa,298K时的热力学数据:
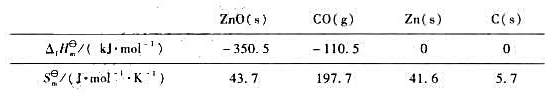
(1)试通过热力学计算,说明下面反应298K时的进行方向:
ZnO(s)+C(s)=Zn(s)+CO(g)
(2)求算上面反应自发正向进行的最低温度。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知下列100kPa,298K时的热力学数据:
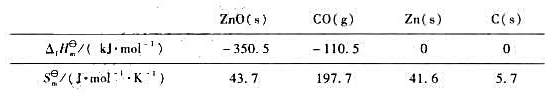
(1)试通过热力学计算,说明下面反应298K时的进行方向:
ZnO(s)+C(s)=Zn(s)+CO(g)
(2)求算上面反应自发正向进行的最低温度。
 答案
答案
 更多“已知下列100kPa,298K时的热力学数据: (1)试通过热力学计算,说明下面反应298K时的进行方向: ”相关的问题
更多“已知下列100kPa,298K时的热力学数据: (1)试通过热力学计算,说明下面反应298K时的进行方向: ”相关的问题
第1题
已知下列各反应298K时的自由能改变量:
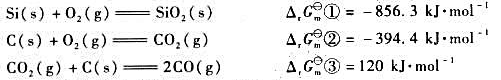
(1)试通过计算说明,制备单质Si的反应:
SiO2(s)+2C(s)=Si(s)+2CO(g)
在常温下不能自发进行。
(2)查热力学数据表,计算上述制备反应的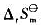 ,进一步计算该反应进行的最低温度要求。
,进一步计算该反应进行的最低温度要求。
第2题
电池Mo(S)|MoS2(S)|H2S(100kPa)|KCl(0.01mol/kg)|HCl(0.01mol/kg)|H2(100kPa)|Pt,测得其在不同温度下的电池电动势数据为 T/K 288 298 308 E/V 0.4148 0.4119 0.4087 (1)写出电极反应和电池反应; (2)由题给数据推导出电池反应的平衡常数与温度的关系式,并计算△rHm; (3)用电化学方法计算298K时电池反应的△rSm,将其与热力学方法计算所得结果相比较可得出什么结论?298K时,物质的规定熵数据为 物质 H(g)H2S(g) Mo(s) MoS2(s) Sm/[J/(K.mol)] 130.6 205.6 28.58 62.59
第3题
已知CH4(g)+2O2(g)=CO2(g)+2H2O(g)反应的热力学数据:△rHΘm(298K)=-802.3 kJmol-1,△fHΘm(CO2,298K)=-393.5KJmol-1,△fHΘm(H2O,g,298K)=-241.82KJmol-1,求△fHΘm(CH4,g,298K)=?
第6题
第7题
已知25℃下列热力学常数:
| Delta _fH_m^{ominus }/(kJcdot mol^{-1}) | S_m^{ominus }/(Jcdot mol^{-1}cdot K^{-1}) | |
| AgCl Ag+ Cl- | -127.0 105.6 -167.2 | 96.3 72.7 56.7 |
求100℃时AgCl的Ksp和在纯水中的摩尔溶解度。
第9题
298K时,已知 =0.799V,
=0.799V, =0.373V,试计算Ag(NH3)2;的络合平衡常数
=0.373V,试计算Ag(NH3)2;的络合平衡常数
第10题
已知298K时,P4O10(s)的,则反应4P(红,s)+5O2(g)====P4O10(s)的
______kJ·mol-1。
第11题
已知298K时某一元弱酸的浓度为0.010mol·L-1,测得其pH为4.00,计算Ka和α。
已知298K时某一元弱酸的浓度为0.010mol·L-1,测得其pH为4.00,计算Ka和α。