 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
计算下列溶液的H+或OH-浓度及pH。
计算下列溶液的H+或OH-浓度及pH。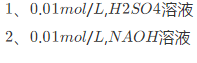
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
计算下列溶液的H+或OH-浓度及pH。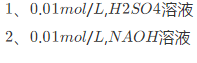
 答案
答案
 更多“计算下列溶液的H+或OH-浓度及pH。”相关的问题
更多“计算下列溶液的H+或OH-浓度及pH。”相关的问题
第1题
A.1.0mol/LNa2CO3溶液中:c(Na+)=2[c(CO32-)+c(HCO3-)+c(H2CO3)]
B.常温下等物质的量浓度的盐酸和NaOH溶液等体积混合后,其溶液的pH恰好等于7
C.物质的量浓度相等CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)+c(OH-)=c(H+)+c(Na+)
D.等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液中:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-)
第2题
试求算0.20mol·dm-3氨水中OH-的浓度,H+的浓度和溶液的pH。向其中加人固体NH4Cl,使NH4+的浓度达到1.0×10-2mol·dm-3,再求体系中OH-的浓度和pH。已知氨水的Kb=1.8×10-5.
第3题
乙二胺(H2NCH2CH2NH2)是二元弱碱,在水中的电离原理类似于氨。常温下,向乙二胺溶液中滴加稀盐酸,溶液的pH随离子浓度变化关系如图所示。下列叙述不正确的是()。
A.Kb2(H2NCH2CH2NH2)的数量级为10-8
B.曲线G代表pH与的变化关系
C.H3NCH2CH2NH2Cl溶液中c(H+)>c(OH-)
D.0.01mol•L-1H2NCH2CH2NH2电离度约为10%
第4题
已知25℃时,Ka(HAc)=1.75×10-5。计算该温度下0.10mol·L-1HAc溶液中H+浓度及溶液的pH,并计算该浓度下HAc的解离度。
第5题
A.(Na+)-c(X-)=9.9×10-7 mol•L-1
B.(Na+)=c(X-)+c(HX)=0.2 mol•L-1
C.(OH-)-c(HX)=c(H+)=1×10-6 mol•L-1
D.(Na+)>c(X-)>c(HX)>c(OH-)>c(H+)
第7题
pH=4的溶液中,[H+]=______mol/L,[OH-]=______mol/L,溶液显______性。
第8题
A.溶液中导电粒子的数目减少
B.溶液中c(CH3COO-)/c(CH3COOH).c(OH-)不变
C.醋酸的电离程度增大,c(H+)亦增大
D.再加入10 mL pH=11的NaOH溶液,混合液pH=7
第9题
pH一4的溶液中,[H+]=______mol/L,[OH-]=______mol/L,溶液显______性。