 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
确定下列反应中的共轭酸碱对,计算反应的标准平衡常数并判断在标准状态下反应进行的方向.
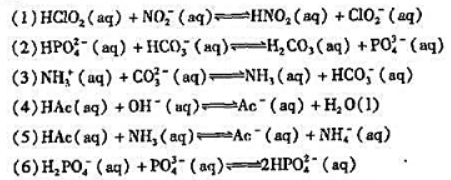
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
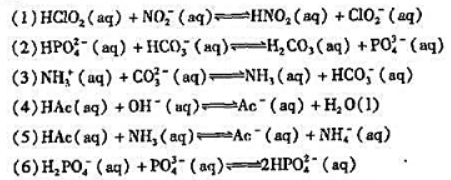
 答案
答案
 更多“确定下列反应中的共轭酸碱对,计算反应的标准平衡常数并判断在标准状态下反应进行的方向.”相关的问题
更多“确定下列反应中的共轭酸碱对,计算反应的标准平衡常数并判断在标准状态下反应进行的方向.”相关的问题
第1题
称取含Na2S和Sb2S3试样0.2000g溶于浓盐酸中,反应生成的H2S用50.00mL0.01000mol/L的I2标液吸收(使H2S→S),然后用0.02000mol/L的Na2S2O3标液滴定剩余的I2,用去10.00mL;此后将试液(已除去H2S)调至微碱性,再用上述I2标液滴定Sb(Ⅲ),耗用10.00mL,试计算试样中Sb2S3与Na2S的质量分数。已知M(Na2S)=78.04g/mol,M(Sb2S3)=339.7g/mol。
第2题
称取锰矿试样1.000g,用Na2O2熔融后,得Na2MnO4溶液。煮沸除去过氧化物后酸化,此时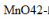 歧化为
歧化为 和MnO2,滤去MnO2,滤液与0.1000mol/L的Fe2+标液反应,消耗了25.00mL。计算试样中MnO的质量分数。
和MnO2,滤去MnO2,滤液与0.1000mol/L的Fe2+标液反应,消耗了25.00mL。计算试样中MnO的质量分数。
第3题
A.沉淀反应要迅速、定量地完成
B.沉淀的溶解度要不受外界条件的影响
C.沉淀不应有显著的吸附现象产生
D.要有确定滴定反应终点的方法
E.沉淀滴定反应产物要有颜色
第5题
H2O2+Br2+2H+==2Br-+O2
作用10min后,赶去过量的Br2,再以0.3162mol·L-1溶液滴定上述反应产生的H+.需17.08mL达到终点,计算瓶中H2O2的含量(以g/100mL表示).
第6题
A.活度比中的分子为氧化型物质,分母为还原型物质
B.活度比中的分子为还原型物质,分母为氧化型物质
C.活度的指数为电极反应中相应反应物的系数
D.电极反应平衡式左右两边所有参与反应的物质活度都应写进计算式,但水和固体物质除外
E.液体和固体物质的活度均为1
第7题
合成氨反应:

在30.4MPa,500℃时,K为7.8×10-5,计算该温度时下列反应的K:
第8题
在容积为3.0L的密闭容器中,装有CO2和H2混合物,存在下列可逆反应:

如果在此密闭容器中混合1.5mol CO2和4.5mol H2,并加热到1123K时,反应达到平衡(已知此时Kc=1.0),计算:
第10题
如图所示,无摩擦、无质量、无体积的活塞1,2,3将反应器隔成甲、乙、丙3部分,分别进行反应
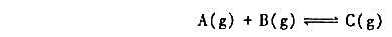
起始时物质的量已标在图中。某温度和100kPa下实现平衡时,各部分的体积分别为V甲,V乙,V丙。
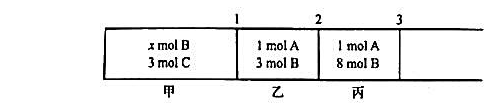
(1)这时若去掉活塞1,不会引起其他活塞移动,求算x值;
(2)去掉活塞2后再次达到平衡时,活塞3向哪个方向发生了移动?试通
过计算加以解释,可以假定反应的Kθ等于1。