 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
称取0.5000g白云石样品,溶于酸后定容成250mL,吸取25.00mL,加掩蔽剂消除干扰,在pH=10时用K~B混合指示剂,以0.
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
 更多“称取0.5000g白云石样品,溶于酸后定容成250mL,吸取25.00mL,加掩蔽剂消除干扰,在pH=10时用K~B混合指示剂,以0.”相关的问题
更多“称取0.5000g白云石样品,溶于酸后定容成250mL,吸取25.00mL,加掩蔽剂消除干扰,在pH=10时用K~B混合指示剂,以0.”相关的问题
第1题
试剂厂生产的FeCl3·6H2O试剂,国家规定二级产品的含量不低于99.0%,三级品含量不低于98.0%。为检验产品质量,称取0.5000g样品。溶于水后,加3mL HCl和2gKI,最后用c(Na2S2O3)=0.1000mol/L的Na2S2O3标准滴定溶液滴定,消耗18.17mL,问该产品属于哪一级?
第2题
准确称取铁矿石试样0.5000g,用酸溶解后加入SnCl2,使Fe3+还原为Fe2+,滴定Fe2+消耗24.50mLKMnO4标准溶液滴定,已知1mL.KMnO4相当于0.01260gH2C2O4·2H2O,(1)矿样中Fe及Fe2O3的质量分数各为多少?(2)取市售双氧水3.00mL,稀释定容于250.00mL,从中取出20.00mL试液,需用上述溶液KMnO421.18mL滴定至终点,计算每100.0mL市售双氧水所含H2O2的质量.
第3题
称取含有KI的试样0.5000g,溶于水后先用Cl2水氧化I-为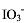 ,煮沸除去过量Cl2;再加入过量KI试剂,滴定I2时消耗了0.02082mol/L Na2S2O321.30mL。计算试样中KI的质量分数。
,煮沸除去过量Cl2;再加入过量KI试剂,滴定I2时消耗了0.02082mol/L Na2S2O321.30mL。计算试样中KI的质量分数。
第4题
称取含BaCl2试样0.5000g,溶于水后加25.00mL 0.05000mol/L KIO3将Ba2+沉淀为Ba(IO3)2,滤去沉淀,洗涤,加入过量KI于滤液中并酸化,滴定析出的I2,消耗0.1000mol/L的Na2S2O3标准溶液21.18mL。写出有关反应方程式,计算BaCl2的百分含量?(MBaCl2=208.27)
第5题
5.00×10-5mol·L-1KMnO4溶液在520nm波长处用2.0cm比色皿测得吸光度A=0.224。称取钢样0.500g,溶于酸后,将其中的Mn氧化成MnO4,定容100.00mL后,在上述相同条件下测得吸光度为0.314。求钢样中锰的质量分数。
第6题
.00mLc(AgNO3)=0.1043mol/LAgNO3溶液,沉淀完全后加入5mL邻苯二甲酸二丁酯,用c(NH4SCN)=0.1015mol/L标准溶液回滴,用去21.45mL,计算烧碱中NaCl的含量。
第7题
用火焰原子吸收分光光度法测土壤中镍。称取风干过筛土样0.5000g(含水7.2%),经消解后定容至50.0mL,用标准曲线法测得此溶液镍含量为30.0μg,求被测土壤中镍含量。
第8题
的比色皿,在波长520nm处测得吸光度为0.620,高锰酸根离子在波长520nm处的摩尔吸收系数为2.24×103。计算钢样中锰的质量分数。(Ar(Mn)=54.94)
第9题
第10题