 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
现有硅酸盐试样1.000g,用重量法测定其中铁及铝时,得到Fe2O3+Al2O3沉淀共重
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
 更多“现有硅酸盐试样1.000g,用重量法测定其中铁及铝时,得到Fe2O3+Al2O3沉淀共重”相关的问题
更多“现有硅酸盐试样1.000g,用重量法测定其中铁及铝时,得到Fe2O3+Al2O3沉淀共重”相关的问题
第1题
某硅酸盐试样1.000g,用重量法测得Fe2O3和Al2O3的总量为0.5000g。将沉淀溶解在酸性溶液中,并将Fe3+还原为Fe2+,然后用0.03000mol/L K2Cr2O7溶液滴定,用去25.00mL。计算试样中FeO和Al2O3的质量分数。
第2题
ol/L NaOH溶液50.00mL溶解沉淀。过量的NaOH用0.2000mol/L HNO3滴定,以酚酞作指示剂,用去HNO310.27mL,计算试样中的磷和五氧化二磷的质量分数。
第3题
第4题
用KMnO4法测定硅酸盐样品中Ca2+的含量,称取试样0.5863g,在一定条件下,将钙沉淀为CaC2O4,过滤、洗涤沉淀,将洗净的CaC2O4溶于稀H2SO4中,用c(KMnO4)=0.05052mol/L的KMnO4标准滴定溶液滴定,消耗25.60mL,计算硅酸盐中Ca的质量分数。
第5题
K2SiF6+3H2O→2KF+HeSiO3+4HF
HF+NaOH→NaF+H2O则SiO2与NaOH物质的量之间的关系应为( )。
A.n(SiO2)=4n(NaOH) B.n(SiO2)=
C.n(SiO2)=n(NaOH) D.n(SiO2)=
E.n(SiO2)=6n(NaOH)
第7题
A.#图片0$#
B.#图片1$#
C.#图片2$#
D.#图片3$#
第8题
称取锰矿试样1.000g,用Na2O2熔融后,得Na2MnO4溶液。煮沸除去过氧化物后酸化,此时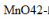 歧化为
歧化为 和MnO2,滤去MnO2,滤液与0.1000mol/L的Fe2+标液反应,消耗了25.00mL。计算试样中MnO的质量分数。
和MnO2,滤去MnO2,滤液与0.1000mol/L的Fe2+标液反应,消耗了25.00mL。计算试样中MnO的质量分数。
第9题
称取Na3PO4和Na2HPO4的混合试样1.000g,溶于适量水后,以百里酚酞为指示剂,用c(HCl)=0.2000mol/L盐酸标准滴定溶液滴定至终点,消耗15.00mL,再加入甲基红指示剂,继续用盐酸标准滴定溶液滴定至终点,又消耗20.00mL,计算混合试样中Na2HPO4的质量分数。
A 7.1% B 3.55% C 10.65% D 14.2%
第10题
测定某试样中锰和钒的含量,称取试样1.000g,溶解后,还原成Mn2+和Vo2+,用0.0200mol/L KMnO4溶液滴定,消耗2.50mL;加入焦磷酸(使Mn3+形成稳定的焦磷酸络合物),继续用上述KMnO4溶液滴定生成的Mn2+和原有的Mn2+到Mn3+,又用去KMnO44.00mL。计算试样中锰和钒的质量分数。
第11题
称取某试样1.000g,将其中的铵盐在催化剂存在下氧化为NO,NO再氧化为NO2,NO2溶于水后形成HNO3。此HNO3用0.01000mol/L NaOH溶液滴定,用去20.00mL。求试样中NH3的质量分数。(提示:NO2溶于水时,发生歧化反应3NO2+H2O→2HNO3+NO↑)