 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
合成氨所用H2的一般制法为:让H2O(g)先通过1000℃以上的煤炭,生成水煤气(CO和H2的混合气体),然后再
合成氨所用H2的一般制法为:让H2O(g)先通过1000℃以上的煤炭,生成水煤气(CO和H2的混合气体),然后再让H2O(g)和水煤气在400℃左右催化生成更多的H2。写出有关的反应方程式。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
合成氨所用H2的一般制法为:让H2O(g)先通过1000℃以上的煤炭,生成水煤气(CO和H2的混合气体),然后再让H2O(g)和水煤气在400℃左右催化生成更多的H2。写出有关的反应方程式。
 答案
答案
 更多“合成氨所用H2的一般制法为:让H2O(g)先通过1000℃以上的煤炭,生成水煤气(CO和H2的混合气体),然后再”相关的问题
更多“合成氨所用H2的一般制法为:让H2O(g)先通过1000℃以上的煤炭,生成水煤气(CO和H2的混合气体),然后再”相关的问题
第2题
A.ΔrHmθ为H2O(g)的生成热
B.ΔrHmθ为H2(g)的燃烧热
C.ΔrHmθ是负值
D.加压有利于该平衡反应向右进行
第4题
反应C(s)+H2O(g)=CO(g)+H2(g),为提高C(s)的转化率,可采取()措施。
A.增加C(s)的用量
B.增加H2O(g)的浓度
C.按1:1增加,C(s)和H2O(g)的用量
D.以上三种方法都可以
第5题
合成氨反应为3H2(g)+N2(g)∩2NH3(g),所用反应物氢气和氮气的摩尔比为3:1,在673K、1000kPa压力下达成平衡,平衡产物中氨的摩尔分数为0.0385。试求:(1)该反应在该条件下的标准平衡常数;(2)在该温度下,若要使氨的摩尔分数为0.05,应控制总压为多少。
第6题
第7题
试用热力学数据表计算823K下以下反应的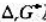 及
及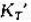 :
:
(1)CoO(s)+H2(g)=Co(s)+H2O(g)
(2)CoO(s)+CO(g)=Co(s)+CO2(g)
并讨论H2和CO还原CoO为Co的可能性,你以为哪种方法更好一些?为什么?
第8题
反应2NO(g)+H2(g)→N2O(g)+ H2O(g)的速率方程为

反应在恒温、恒容的条件下进行,测得实验数据如下:
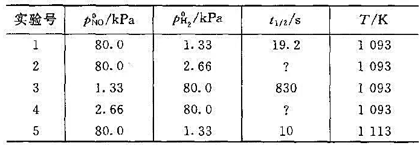
(1)求所缺的半衰期数据;(2)求1093 K时的速率常数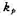 ;(3)求反应的活化能
;(3)求反应的活化能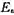 ;(4)提出一个只涉及双分子步骤的反应机理,由此机理可得上述规律;(5)如果1093K时,
;(4)提出一个只涉及双分子步骤的反应机理,由此机理可得上述规律;(5)如果1093K时,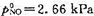 ,
,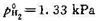 ,求该反应的半衰期。
,求该反应的半衰期。
第9题
A.1:1:1
B.1:0.5:0.33
C.2:1:0.66
D.不能确定
第10题
A.K1+K2+K3
B.K1-K2-K3
C.K1K2K3
D.K1K3/K2