 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
PCl5的分解反应:PCl5(g)=PCl3(g)+Cl2(g),在473K达到平衡时PCl5(g)有48.5%分解,在573K达到平衡时,有97%分解。可知该分解反应()。
A.吸热
B.放热
C.没有热效应
D.无法确定
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.吸热
B.放热
C.没有热效应
D.无法确定
 答案
答案
 更多“PCl5的分解反应:PCl5(g)=PCl3(g)+Cl2(g),在473K达到平衡时PCl5(g)有48.5%分解,在573K达到平衡时,有97%分解。可知该分解反应()。”相关的问题
更多“PCl5的分解反应:PCl5(g)=PCl3(g)+Cl2(g),在473K达到平衡时PCl5(g)有48.5%分解,在573K达到平衡时,有97%分解。可知该分解反应()。”相关的问题
第1题
已知PCl5的热分解反应:
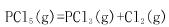
某温度时,在容积为10L的密闭容器中的2mol PCl5有1.5mol分解了,计算此温度时的平衡常数Kc。
第2题
PCl5的分解反应为
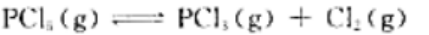 升高温度时,PCl5的分解百分率增大。试回答下列问题:
升高温度时,PCl5的分解百分率增大。试回答下列问题:
(1)PCl5分解反应是吸热反应还是放热反应?
(2)在恒温时,缩小反应容器的体积增大压力,PCl5分解百分率有何影响?
第3题
在250℃时,PCl5依下式分解建立平衡:
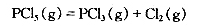
(1)在2.00L密闭容器中加人0.700molPCl5,平衡时分解了0.5mol,求此时的Kr,Kp及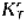 以及反应的
以及反应的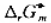 .
.
(2)若再往容器中加入0.100molCl2,PCl5的分解率将是多少?
第4题
偶氮甲烷(CH3NNCH3)气体的分解反应
(CH3NNCH3)(g)→C2H6(g)+N2(g).
为一级反应.在287℃的真空密闭恒容容器中充入初始压力为21.332kPa的偶氮甲烷气体,反应进行1000s时测得系统的总压为22.732kPa,求速率常数k及半衰期t1/2.
第6题
℃下,每升气体会产生3.5×1029次·s-1的碰撞,如果每次碰撞都会发生化学反应,试计算HI的分解反应的速率.实验测定,该反应实际的反应速率是1.2×10-8·mol·dm-3·s-1,试求HI气体中活化分子的百分数(设每次活化分子的相互碰撞都产生反应).
第7题
1100K时NH3(g)在w上的分解数据如下:

试证明此反应为零级反应,求平均k.
第8题
在67℃时,获得N2O5(g)分解反应
| t/s | 0.0 | 60.0 | 120.0 | 180.0 | 240.0 |
| c(N2O5)/(mol·L-1) | 0.160 | 0.113 | 0.080 | 0.056 | 0.040 |
第10题
A.239.2kJ
B.438.4kJ
C.119.6kJ
D.358.8kJ
第11题
Fe3+可以作为H2O2歧化(分解)反应的催化剂.若该反应的机理为
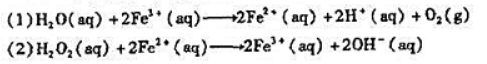
总反应:2H2O2(aq)→2H2O(l)+O2(g)
查出相关电对的标准电极电势,说明上述机理的可行性.并推断Ca2+催化H2O2分解的反应机理.