 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
煤液化反应总体是()热反应。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
 更多“煤液化反应总体是()热反应。”相关的问题
更多“煤液化反应总体是()热反应。”相关的问题
第1题
煤和由煤与水蒸气反应[C(s)+H2O(g)=H2(g)+CO(g)]而得的水煤气(CO与H2等物质的混合物)都可用做燃料。设煤含碳80%,其余可燃成分忽略不计。试通过计算说明,在实际应用中以水煤气代替煤作燃料的优点。(提示:在任何能量转换过程中,总会有一些能量变成热而扩散到环境中。例如,欲往某体系输入xkJ的能量,实际上提供的热量要远多于该值。)
第2题
(1)对于安全问题,我们一定要高度重视,绝对不能麻痹大意,更不能在发生事故以后摆出各种各样的理由__________责任。
(2)这次“全运会”,北京运动员的总体成绩有了明显的提高,分析其原因,主要是__________教练训练指导有方。
(3)日前,一种新型的环保电脑在一片热捧声中__________,消费者却对此反应十分冷谈,问津者寥寥无几。
填入横线部分最恰当的一项是()。

第5题
第8题
反应
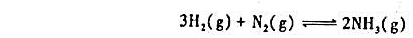
200℃时标准平衡常数 = 0.64,400℃时标准平衡常数
= 0.64,400℃时标准平衡常数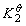 =6.0×10-4,据该反应的标准摩尔反应热
=6.0×10-4,据该反应的标准摩尔反应热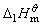 和NH3(g)的标准摩尔生成热
和NH3(g)的标准摩尔生成热 。
。
第10题
CH3I反应,再与湿Ag2O反应,热解产生中间体C10H21N,后者进一步甲基化转变为氢氧化物,再热解生成三甲胺、1,5-辛二烯和1,4-辛二烯。试推测毒芹碱和中间体的结构。
第11题
甲醇(CH3OH)是一种具有高辛烷值并能完全燃烧的“新型燃料”,可以用氢和煤人工制造。 根据: (1)CH3OH(l)+1/2O2(g)=C(石墨)+2H2O(l),△rHΘm=-333.00KJmol-1 (2)C(石墨)+1/2O2(g)=CO(g),△rHΘm=-111.52 kJmol-1 (3)H2(g)+1/2O2(g)——H2O(l),△rHΘm=-285.83 kJmol-1 计算反应(4)2H2(g)+CO(g)=CH3OH(l)的△rHΘm。