题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在800K和100kPa下,将8.0molSO2和4.0molO2加入到含有催化剂MnO2的密闭容器中,在
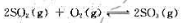
反应达到平衡时,测得混合物中有6.0molSO2(g)。试计算:
(1)该可逆反应在800K时的标准平衡常数和标准摩尔吉布斯自由能变;
(2)SO2在上述条件下的平衡转化率。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
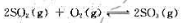
反应达到平衡时,测得混合物中有6.0molSO2(g)。试计算:
(1)该可逆反应在800K时的标准平衡常数和标准摩尔吉布斯自由能变;
(2)SO2在上述条件下的平衡转化率。
 答案
答案
 更多“在800K和100kPa下,将8.0molSO2和4.0molO2加入到含有催化剂MnO2的密闭容器中,在”相关的问题
更多“在800K和100kPa下,将8.0molSO2和4.0molO2加入到含有催化剂MnO2的密闭容器中,在”相关的问题
第2题
在一定温度下,将1.0molNa2O2(g)放入一密闭容器中,发生下列可逆反应
 当达到化学平衡时,容器内有0.8molNO,气体总压为100kPa。则该可逆反应在此温度下的标准平衡常数为().
当达到化学平衡时,容器内有0.8molNO,气体总压为100kPa。则该可逆反应在此温度下的标准平衡常数为().
A、0.40
B、0.67
C、0.76
D、1.3
第3题
某种类型的煤含硫为3.0%(质量分数),问: (1)燃烧100g该种煤,将产生多少克二氧化硫? (2)在298K与100kPa下,将产生多少体积的SO2? (3)如采用1.00m3空气燃烧这部分煤,烟道气中SO2的浓度为多少?
第5题
反应2A(g)+B(g)====2C(g),在700K和800K时Kp分别为1.0×105和1.2×102。此反应是吸热反应还是放热反应?
第6题
体,而是黑度为0.8的实际表面,两表面温度仍为800K和400K,试求其黑度。
第7题
A.纯理想气体的标准状态就是标准压力P(100KPa)下的状态
B.纯液体物质的标准状态就是标准压力P(100KPa)下的纯液体
C.纯固体物质的标准状态就是标准压力P(100KPa)下的纯固体
D.不同的物质在相同温度下都处于标准状态时,它们的同一热力学函数值都应相同
第8题
已知某种土剪切试验结果如下:在法向应力100kPa、200kPa、300kPa、400kPa作用下,所测得的峰值抗剪强度为τf=105kPa、151kPa、207kPa、260kPa,终值抗剪强度为τf=34kPa、65kPa、93kPa、103kPa。
第9题
电池Mo(S)|MoS2(S)|H2S(100kPa)|KCl(0.01mol/kg)|HCl(0.01mol/kg)|H2(100kPa)|Pt,测得其在不同温度下的电池电动势数据为 T/K 288 298 308 E/V 0.4148 0.4119 0.4087 (1)写出电极反应和电池反应; (2)由题给数据推导出电池反应的平衡常数与温度的关系式,并计算△rHm; (3)用电化学方法计算298K时电池反应的△rSm,将其与热力学方法计算所得结果相比较可得出什么结论?298K时,物质的规定熵数据为 物质 H(g)H2S(g) Mo(s) MoS2(s) Sm/[J/(K.mol)] 130.6 205.6 28.58 62.59
第10题
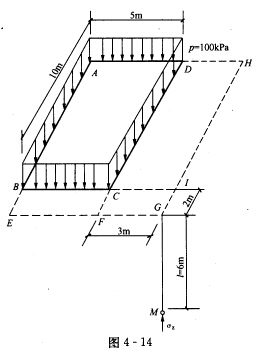
如图4—14所示矩形面积(ABCD)上作用均布荷载p=100kPa,试用角点法计算G点下深度6m处M点的附加应力值σz。