 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
铅酸著电池的电极反应为负极:正极:(1)计算铅酸费电池的标准电动势.(2)如果将6个(1)中的铅酸蓄
铅酸著电池的电极反应为
负极: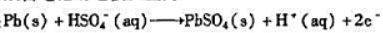
正极: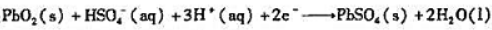
(1)计算铅酸费电池的标准电动势.
(2)如果将6个(1)中的铅酸蓄电池串连在一起,其总电动势为多少?
(3)充电时的电极反应如何?写出相应的反应方程式.
(4)在使用过程中,可用测定硫酸密度的方法,确定铅酸蓄电池是否需要充电,这是什么道理?
(5)充电时,需要用新的浓度大的硫酸咎换电池中的稀硫酸吗?为什么?
 答案
答案





 在酸性溶液中的半反应为
在酸性溶液中的半反应为 ,试计算在c(H+)=1.0mol/L,c(
,试计算在c(H+)=1.0mol/L,c(



















