 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
试解释Fe与盐酸作用产物和Fe与氯气作用产物不同的原因。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
 更多“试解释Fe与盐酸作用产物和Fe与氯气作用产物不同的原因。”相关的问题
更多“试解释Fe与盐酸作用产物和Fe与氯气作用产物不同的原因。”相关的问题
第1题
解释以下事实:
(1)单质铁与盐酸作用的产物是FeCl2,但在与氯气反应时的产物是FeCl3.
(2)单质银没有氢活泼,但Ag可从Hl溶液中置换出氢气.
(3)硝酸钠或稀硫酸溶液都没有明显的氧化性,例如,它们都不可能氧化Fe2+为Fe3+,但二者结合后都可以使Fe2+氧化为Fe3+.
(4)久置于空气的H2S溶液会变浑浊.
(5)Fel3,Cul2等化合物不存在.
(6)在碱性溶液条件下,金属铁可得到暂时性保护.
(7)用简单的锌盐及铜盐混合液进行电镀时,锌和铜不会同时析出.但在混合离子溶液中加入NaCN溶液,可使Cu,Zn同时析出.
第2题
(1)Fe3O4粉末在复印机的电磁场作用下能使墨粉形成字迹或图案,这不仅利用了Fe3O4有磁性,还利用了Fe3O4是()色。 (2)铁的氧化物一般都可以与盐酸反应,氧化亚铁与盐酸反应方程式为(),四氧化三铁与盐酸反应方程式为()。 (3)第②步加入试剂X,试剂X的名称是()。 (4)在第③步反应是要向溶液中通入O2,以使生成的Fe(OH)2部分转化成Fe(OH)3,写出反应的化学方程式()。在第③步反应中要控制通入O2的量,以使生成的Fe(OH)2和Fe(OH)3的质量比等于(),才能确保第④步反应最终完全反应生成Fe3O4。(5)操作Y的流程为()、()、晾干。
第3题
高铁酸钾是一种高效的多功能水处理剂,具有氧化、吸附、絮凝、、助凝、杀菌、除臭等作用,高铁酸钾的开发和利用正日益显示出其广阔的应用前景。其制备路线如下: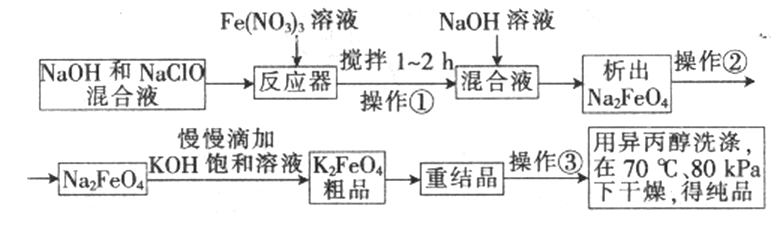
试答复以下问题:
问题一、操作①搅拌的目的是:()。
问题二、操作②与操作③相同,该操作名称是:()。
问题三、反应器中,NaOH、NaClO及Fe(NO3)3反应的离子方程式为:()。
问题四、次氯酸钠浓度对高铁酸钾产率有一定影响,当高铁酸钾产率最高时,NaClO的物质的量浓度约为()。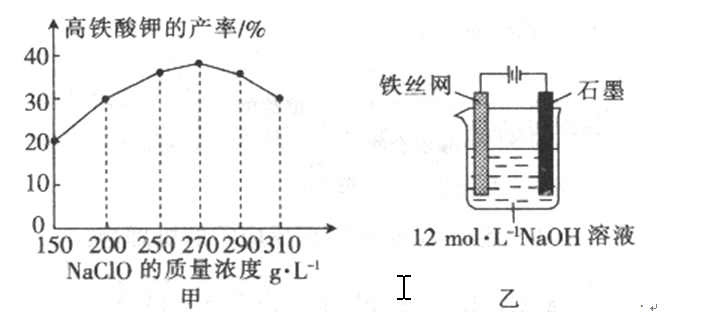
问题五、从环境保护的角度看,制备中间产物Na2FeO4较好的方法为电化学法,其装置如图乙所示,则阳极的电极反应式为()。
第4题
Fe3+的配位化合物[Fe(CN)6]3-比Fe2+的配位化合物[Fe(CN)6]4-
稳定,但与邻二氮菲![Fe3+的配位化合物[Fe(CN)6]3-比Fe2+的配位化合物[Fe(CN)6]4-⊕Fe3+的配](https://img2.soutiyun.com/ask/2020-11-12/974068963703785.png) (简写成phen)生成的配位化合物
(简写成phen)生成的配位化合物
[Fe(phen)3]3+不如Fe(phen)3]2+稳定。试解释其原因。
第7题
下列金属中,与硝酸反应得到产物的氧化数最低是
(A) In; (B) Tl; (C) Fe; (D) Bi。
第8题
推理判断:
某盐(A)与盐酸反应,生成(B)的溶液和气体(C)。向(B)的浓溶液中加锑酸钾,析出白色晶状沉淀(D)。将气体(C)通入碘化钾溶液,生成(E)和(F),(E)使溶液发黄,(F)与过量硝酸铅生成白色沉淀(C),(G)溶于过量氢氧化钠溶液得(H),(H)与(A)反应生成黑色沉淀(I)。(I)加到硫酸锰溶液中可使溶液变成紫红色,说明有离子(J)生成。
试给出(A),(B),(C),(D),(E),(F),(G),(H),(I)和(J)的化学式,并完成各步的化学反应方程式。
(2)白色固体(A)高温下分解成(B)和气体(C)。白色固体(B)与碳在更高的温度下共热生成(D),灰黑色固体(D)与水作用生成重要工业燃气(E)和化合物(F)。(B)与稀盐酸反应生成(G)的溶液。电解(G)的无水熔盐得(H)和气体(I)。金属(H)在高温下与(J)化合成为(K),白色晶体(K)与水反应的产物中有(F)。气体(J)在(I)中燃烧的产物溶于水得盐酸。(D)在高温下与水蒸气作用,其固体产物为(A),气体产物为(C)和(J)。
试给出(A),(B),(C),(D),(E),(F),(G),(H),(I),(J)和(K)的化学式,并完成各步的化学反应方程式。
第9题
Fe3O4与盐酸作用的产物为 ()
A.FeCl3+H2O
B.FeCl2+H2O
C.FeCl3+FeCl2+H2O
D.FeCl3+Cl2