 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在298K时,反应O3(g)+NO(g)=O2(g)+NO2(g)的活化能为10.6kJ·mol-1,如果加入催化剂,使活化能减小到5.3kJ·mol-1,在不改变其他条件下,该反应的反应速率大约是加入催化剂前的多少倍()?
A.0.693倍
B.137倍
C.8.5倍
D.2倍
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.0.693倍
B.137倍
C.8.5倍
D.2倍
 答案
答案
 更多“在298K时,反应O3(g)+NO(g)=O2(g)+NO2(g)的活化能为10.6kJ·mol-1,如果加入催化剂,使活化能减小到5.3kJ·mol-1,在不改变其他条件下,该反应的反应速率大约是加…”相关的问题
更多“在298K时,反应O3(g)+NO(g)=O2(g)+NO2(g)的活化能为10.6kJ·mol-1,如果加入催化剂,使活化能减小到5.3kJ·mol-1,在不改变其他条件下,该反应的反应速率大约是加…”相关的问题
第1题
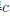 (H2O,1)=-237kJ·mol-1,则反应2H2(g)+O2(g)
(H2O,1)=-237kJ·mol-1,则反应2H2(g)+O2(g) 2H2O(l)在该温度下的
2H2O(l)在该温度下的 为( )。
为( )。A.1.2×1083
B.3.5×1041
C.2.7×10-42
D.7.5×10-84
第2题
已知298K时,P4O10(s)的,则反应4P(红,s)+5O2(g)====P4O10(s)的
______kJ·mol-1。
第3题
电池Mo(S)|MoS2(S)|H2S(100kPa)|KCl(0.01mol/kg)|HCl(0.01mol/kg)|H2(100kPa)|Pt,测得其在不同温度下的电池电动势数据为 T/K 288 298 308 E/V 0.4148 0.4119 0.4087 (1)写出电极反应和电池反应; (2)由题给数据推导出电池反应的平衡常数与温度的关系式,并计算△rHm; (3)用电化学方法计算298K时电池反应的△rSm,将其与热力学方法计算所得结果相比较可得出什么结论?298K时,物质的规定熵数据为 物质 H(g)H2S(g) Mo(s) MoS2(s) Sm/[J/(K.mol)] 130.6 205.6 28.58 62.59
第4题
已知CH4(g)+2O2(g)=CO2(g)+2H2O(g)反应的热力学数据:△rHΘm(298K)=-802.3 kJmol-1,△fHΘm(CO2,298K)=-393.5KJmol-1,△fHΘm(H2O,g,298K)=-241.82KJmol-1,求△fHΘm(CH4,g,298K)=?
第5题
已知反应:2H2(g)+O2(g)=2H2O(g),△fHΘm(H2O,1 298K)=-237.18kdmol-1求该反应的KΘ=___________。
第6题
A.138kPa
B.11.99kPa
C.4.9kPa
D.49kPa
第7题
已知298K时,SrCO3的溶度积为5.6×10-10,则1 L溶液中所能溶解的SrCO3质量为________g(M=147.6g.L-1)。
第8题
Silver oxide,Ag2O,can decompose into its elements,Ag(S)and O2(g).(a)Write a balanced equation for this decomposition reaction.(b)Calculate the
第9题
反应2A(g)+B(g)====2C(g),在700K和800K时Kp分别为1.0×105和1.2×102。此反应是吸热反应还是放热反应?
第10题
已知反应Fe3O4(s)+CO(g)====3FeO(s)+CO2(g)的
第11题
反应C(s)+2H2(g)=CH4(g)在1000K时的ΔGm=19.29kJ当总气压=101kpa,气相组成为:H270%、N210%、N210%的条件下,上述反应:
A正向进行
B平衡
C逆向进行
D不定