题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
氨合成塔入口的气体组成(摩尔分数)为NH33.5%,N220.87%,H262.6%,Ar7.08%及CH45.89%。该塔在30MPa压力下操作。
氨合成塔入口的气体组成(摩尔分数)为NH33.5%,N220.87%,H262.6%,Ar7.08%及CH45.89%。该塔在30MPa压力下操作。已知催化剂床层中某处的温度为490℃,反应气体中氨含量为10%(摩尔分数)。试计算该处的反应速率。在Fe催化剂上氨合成反应速率式为
逆反应的活化能
。450℃时,k2=1.02×105kmol·Pa0.5/(m3·h),且
;490℃时,Kp可按下式计算:
 答案
答案
氨的反应速率r=180.1kmol/(m3·h)。[思路] 首先要由450℃的k2值求出490℃时的k'2值,然后利用平衡常数求得反应温度下的k1值。做法是先利用阿伦尼乌斯方程,求出频率因子A。再计算490℃下的k'2值
利用来求取k1值:
由化学反应式求各组分的分压值。设y为反应后的总物质的量,以100mol为计算基准。列三参数表如下。
| 组分 | 进口含量 | 反应后含量 |
求出反应后的总物质的量y的值。进而求出各组分的摩尔分数及分压值:
| 组分 | 摩尔分数/% | 分压值 |
最后将所有数据代入反应速率式,计算出催化剂床层某处(温度为490℃、氨含量为10%)的反应速率。





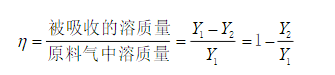
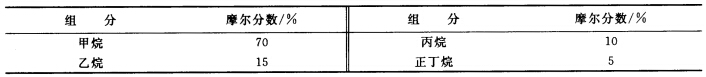 进料气在24℃,0.2026MPa压力下,在板式塔中用烃油吸收,烃油含1%正丁烷,99%不挥发性烃油,进塔的温度和压力与进料气相同。所用液气比为3.5。进料气中的丙烷至少有70%被吸收。甲烷在烃油中的溶解度可以忽略,而其它的组分均形成理想溶液。估算所需的理论级数和出口气相的组成。各组分有关物性数据如下:
进料气在24℃,0.2026MPa压力下,在板式塔中用烃油吸收,烃油含1%正丁烷,99%不挥发性烃油,进塔的温度和压力与进料气相同。所用液气比为3.5。进料气中的丙烷至少有70%被吸收。甲烷在烃油中的溶解度可以忽略,而其它的组分均形成理想溶液。估算所需的理论级数和出口气相的组成。各组分有关物性数据如下: