 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
1mol水蒸气(H2O,g)在100℃,101.325kPa下全部凝结成液态水。求过程的功。
1mol水蒸气(H2O,g)在100℃,101.325kPa下全部凝结成液态水。求过程的功。
 答案
答案
3.102kJ
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
1mol水蒸气(H2O,g)在100℃,101.325kPa下全部凝结成液态水。求过程的功。
 答案
答案
3.102kJ
 更多“1mol水蒸气(H2O,g)在100℃,101.325kPa下全部凝结成液态水。求过程的功。”相关的问题
更多“1mol水蒸气(H2O,g)在100℃,101.325kPa下全部凝结成液态水。求过程的功。”相关的问题
第1题
SƟH2O(g)>(298K)= 188.72J/(K·mol)。
第2题
第3题
计算1mol H2(g)与0.5molO2(g)结合生成H2O(1)所放出的热量。 (2)计算1kg H2完全燃烧放出的热量,并以此与同量的煤(设仅含12C)完全燃烧放出的热量作一比较,得出何种结论?
第4题
已知水(H2O,I)在100℃的饱和蒸气压p=101.325kPa,在此温度.压力下水的摩尔蒸发焓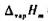 =40.668kJ·mol-1.求在100℃,101.325kPa下使1kg水蒸气全部凝结成液体水时的Q,W,ΔU和ΔH.设水蒸气适用理想气体状态方程.
=40.668kJ·mol-1.求在100℃,101.325kPa下使1kg水蒸气全部凝结成液体水时的Q,W,ΔU和ΔH.设水蒸气适用理想气体状态方程.
第5题
煤和由煤与水蒸气反应[C(s)+H2O(g)=H2(g)+CO(g)]而得的水煤气(CO与H2等物质的混合物)都可用做燃料。设煤含碳80%,其余可燃成分忽略不计。试通过计算说明,在实际应用中以水煤气代替煤作燃料的优点。(提示:在任何能量转换过程中,总会有一些能量变成热而扩散到环境中。例如,欲往某体系输入xkJ的能量,实际上提供的热量要远多于该值。)
第6题
第9题
已知在101.325kPa下,水的沸点为100℃,其比蒸发焓△vaph=2257.4kJ·kg-1。已知液态水和水蒸气在100~120℃范围内的平均比定压热容分别为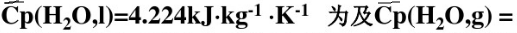
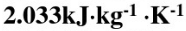 。今有101.325kPa下120℃的1kg过热水变成同样温度、压力下的水蒸气。设计可逆途径,并按可逆途径分别求出过程的△S及△G。
。今有101.325kPa下120℃的1kg过热水变成同样温度、压力下的水蒸气。设计可逆途径,并按可逆途径分别求出过程的△S及△G。
第10题
反应2NaHCO3(s)===Na2CO3(s)+H2O(g)+CO2(g)在不同温度时的平衡总压如表5-3所示。
表5-3 | ||||||
t/℃ | 30 | 50 | 70 | 90 | 100 | 110 |
p/kPa | 0.827 | 3.999 | 15.90 | 55.23 | 97.47 | 167.0 |
设反应的Δr Hm与温度无关。
求:(1)上述反应的ΔrHm;
(2)lg(p/kPa)与T的函数关系;
(3)NaHCO3(s)的分解温度。