 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
实验测得[Co(NH3)6]3+配离子是抗磁性的,试问: (1)它的空间构型是什么?根据价键理论Co3+采用什么样的杂化
实验测得[Co(NH3)6]3+配离子是抗磁性的,试问:
(1)它的空间构型是什么?根据价键理论Co3+采用什么样的杂化轨道与配位体NH3分子形成配位健?
(2)根据晶体场理论绘出此配离子两种可能的d电子构型,表明它们的高低自旋和磁性情况,对此配离子哪种情况是正确的?
(3)当[Co(NH3)6]3+被还原为[Co(NH3)6]2+时,磁矩约为4~5B.M.,绘出其可能的d电子构型,说明它们的磁性情况。
 答案
答案
(1)[Co(NH3)6]3+配离子是抗磁性的,因此配合物中未成对电子的数目为0;Co3+的价层电子构型为3d6,因此其电子层结构为

由于有两个空的d轨道,因此Co3+能够以d2sp3杂化方式形成六个d2sp3杂化轨道与NH3分子形成配位键,分子的空间构型为正八面体构型。
(2)Co3+的d电子在八面体场中的分布:
在弱场中,△o<P

在强场中,△o>P

在弱场中,配合物有四个未成对电子,是高自旋的顺磁性化合物;在强场中,配合物的电子全部配对,是低自旋的抗磁性化合物。而实验测得[Co(NH3)6]3+是3+抗磁性的,因此[Co(NH3)6]件采用强场、低自旋的电子排布。
(3)[Co(NH3)6]2+中Co2+的价层电子构型为3d7,因为配合物的磁矩约为4~5B.M.,因此Co2+的电子层结构可能为

配合物分子中有三个未成对电子,因此具有顺磁性。





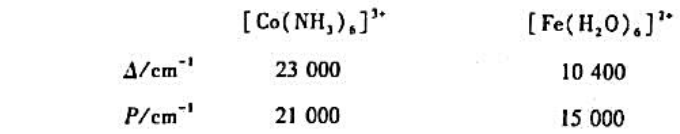
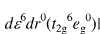 的是()。
的是()。



















