 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在浓度为0.20mol·L-1、体积为100mL的MgCl2溶液中,加入等体积等浓度的氨水, (1)问有无沉淀生成? (2)为阻止
在浓度为0.20mol·L-1、体积为100mL的MgCl2溶液中,加入等体积等浓度的氨水,
(1)问有无沉淀生成?
(2)为阻止沉淀生成,需要加入多少克固体NH4Cl?
 答案
答案
已知Mg(OH)2的Ksp=1.2×10-11。
(1)首先需要计算混合后溶液各自的浓度。
c(氨水)=0.10mol·L-1, c(Mg2+)=0.10mol·L-1
再计算这样浓度的氨水能产生的OH-的浓度为1.3×10-3mol·L-1
最后计算这样浓度的氨水能否产生Mg(OH)2的沉淀:
[Mg2+][OH-]2=0.10×(1.3×10-3)2=1.7×10-7>Mg(OH)2的Ksp=1.2×10-11
所以有Mg(OH)2沉淀生成。
(2)需要NH4Cl的质量至少为:
0.16mol·L-1×53.5g·mol-1×0.2 L=1.7 g





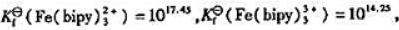 其他数据查附表.
其他数据查附表.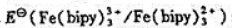 ;
;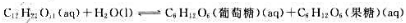 当蔗糖的起始浓度为amol·L-1时,在温度T时水解反应达到平衡时蔗糖水解了1/3,试计算该温度下蔗糖水解反应的标准平衡常数。
当蔗糖的起始浓度为amol·L-1时,在温度T时水解反应达到平衡时蔗糖水解了1/3,试计算该温度下蔗糖水解反应的标准平衡常数。



















