 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在298 K时,醋酸HAc的解离平衡常数 ,试计算在下列不同情况下醋酸在浓度为1.0mol·kg-1时的解离
在298 K时,醋酸HAc的解离平衡常数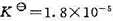 ,试计算在下列不同情况下醋酸在浓度为1.0mol·kg-1时的解离度。(1)设溶液是理想的,活度因子均为1;(2)用Debye-Huckel极限公式计算出γ±的值,然后再计算解离度。设未解离的HAc的活度因子为1.
,试计算在下列不同情况下醋酸在浓度为1.0mol·kg-1时的解离度。(1)设溶液是理想的,活度因子均为1;(2)用Debye-Huckel极限公式计算出γ±的值,然后再计算解离度。设未解离的HAc的活度因子为1.
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在298 K时,醋酸HAc的解离平衡常数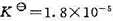 ,试计算在下列不同情况下醋酸在浓度为1.0mol·kg-1时的解离度。(1)设溶液是理想的,活度因子均为1;(2)用Debye-Huckel极限公式计算出γ±的值,然后再计算解离度。设未解离的HAc的活度因子为1.
,试计算在下列不同情况下醋酸在浓度为1.0mol·kg-1时的解离度。(1)设溶液是理想的,活度因子均为1;(2)用Debye-Huckel极限公式计算出γ±的值,然后再计算解离度。设未解离的HAc的活度因子为1.
 答案
答案
 更多“在298 K时,醋酸HAc的解离平衡常数 ,试计算在下列不同情况下醋酸在浓度为1.0mol·kg-1时的解离”相关的问题
更多“在298 K时,醋酸HAc的解离平衡常数 ,试计算在下列不同情况下醋酸在浓度为1.0mol·kg-1时的解离”相关的问题
第1题
某一气相反应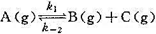 ,已知在298 K时,k1=0.21s-1,k-2=5×10-9Pa-1·s-1,当温度由298 K升到310 K时,k和k-2的值均增加1倍,试求:
,已知在298 K时,k1=0.21s-1,k-2=5×10-9Pa-1·s-1,当温度由298 K升到310 K时,k和k-2的值均增加1倍,试求:
(1)298K时的反应平衡常数Kp;
(2)正、逆反应的实验活化能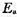 ;
;
(3)298K时反应的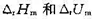 ;
;
(4)在298K时,A的起始压力为100kPa,若使总压力达到152kPa,所需的时间。
第2题
在375K时反应SO2Cl2(g)=SO2(g)+Cl2(g)的标准平衡常数Kθ为2.4。今将5.4g的SO2Cl2(g)置于密闭容器中,并加热到375K。(1) 假定SO2Cl2(g)不解离,它的压力将是多少?(2) 平衡时SO2Cl2(g)、SO2(g)和Cl2(g)的分压各是多少?
第3题
MnS沉淀溶于HAc的反应式如下:MnS+2HAc====Mn2++H2S+2Ac-,计算该反应的平衡常数K。欲使0.010molMnS沉淀完全溶解于1.0LHAc中,计算HAc的最初浓度至少为多少?((MnS)=1.4×10-15,(HAc)=1.8×10-5,H2S:=1.3×10-7,=7.1×1015)
第5题
说明可逆反应的速率常数kt,kt与其平衡常数K之间关系。若已知某温度下氢氟酸解离反应
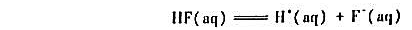
的平衡常数为7.08×10-4mol-1·dm-3,又知基元反应
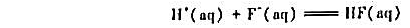
的速率常数为1.00×1011dm3·mol-1·s-1,试求氢氟酸解离反应的速率常数。
第6题
电池Mo(S)|MoS2(S)|H2S(100kPa)|KCl(0.01mol/kg)|HCl(0.01mol/kg)|H2(100kPa)|Pt,测得其在不同温度下的电池电动势数据为 T/K 288 298 308 E/V 0.4148 0.4119 0.4087 (1)写出电极反应和电池反应; (2)由题给数据推导出电池反应的平衡常数与温度的关系式,并计算△rHm; (3)用电化学方法计算298K时电池反应的△rSm,将其与热力学方法计算所得结果相比较可得出什么结论?298K时,物质的规定熵数据为 物质 H(g)H2S(g) Mo(s) MoS2(s) Sm/[J/(K.mol)] 130.6 205.6 28.58 62.59
第9题
已知25℃时,Ka(HAc)=1.75×10-5。计算该温度下0.10mol·L-1HAc溶液中H+浓度及溶液的pH,并计算该浓度下HAc的解离度。