 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知四氧化二氮的分解反应如下:在298.15K时,=4.75kJ·mol-1.试判断在此温度及下列条件下,
已知四氧化二氮的分解反应如下:

在298.15K时,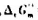 =4.75kJ·mol-1.试判断在此温度及下列条件下,反应进行的方向.
=4.75kJ·mol-1.试判断在此温度及下列条件下,反应进行的方向.
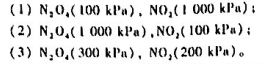
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知四氧化二氮的分解反应如下:

在298.15K时,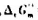 =4.75kJ·mol-1.试判断在此温度及下列条件下,反应进行的方向.
=4.75kJ·mol-1.试判断在此温度及下列条件下,反应进行的方向.
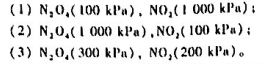
 答案
答案
 更多“已知四氧化二氮的分解反应如下:在298.15K时,=4.75kJ·mol-1.试判断在此温度及下列条件下,”相关的问题
更多“已知四氧化二氮的分解反应如下:在298.15K时,=4.75kJ·mol-1.试判断在此温度及下列条件下,”相关的问题
第1题
二氧化氮被臭氧化生成五氧化二氮.其反应机理如下:
①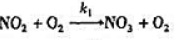 慢
慢
②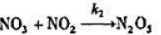 快
快
(1)写出反应方程式及其速率方程;
(2)写出各步反应的活化络合物的结构式及总反应的中间产物的化学式.
第2题
完成并配平下列化学反应方程式.
(1)过氧化钠与冷水作用.
(2)在熔融的条件下三氧化二铬与过氧化钠反应.
(3)二氧化碳与过氧化钠作用.
(4)臭氧化钾溶于水.
(5)金属锂在氧气中燃烧.
(6)用镁还原四氯化钛.
(7)超氧化钾与二氧化碳反应.
(8)硝酸钠在800℃下受热分解.
(9)碳酸镁受热分解.
(10)六水合氯化镁受热分解.
(11)臭氧与氢氧化钾固体作用.
(12)六硝基合钴(Ⅲ)酸钾溶液中加入钠离子.
第3题
已知300K时: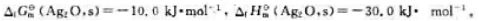
(1)试通过计算说明在300K、标准状态下、Ag2O(s)能否发生如下分解反应:
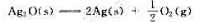
(2)计算在标准状态下Ag2O(s)发生分解反应的最低温度。
第5题
氧化偶氮苯在硫酸(质量分数为0.8822)的催化下转化为羟基偶氮苯,反应过程中定期从反应混合物中取出已知体积的样品,并立即用碱性乙醇溶液终止反应。产物羟基偶氮苯的浓度可通过样品溶液对一定波长(435nm)光的吸收来测定。在确定的波长下,只有产物对光有吸收。反应在298.15K下进行,测得不同反应时间样品吸光度IA的实验数据如下:
| t×103/s | 0.0 | 3.6 | 7.2 | 10.8 | 14.4 | 18.0 |
| IA | 0.007 | 0.134 | 0.250 | 0.343 | 0.416 | 0.476 |
| r×103/s | 21.6 | 27.0 | ∞ | |||
| IA | 0.529 | 0.590 | 0.781 |
已知反应物初始浓度cA0=1.87×10-3mol·dm-3,试确定该反应的级数和速率常数。(提示:若反映反应系统组成的某物理量L满足以下条件:1.具的加和性;2.与浓度成线性关系。则对于不可逆反应,系统组分A的浓度与物理量L满足下列关系式:
式中:L0,It,L∞分别表示0,t,∞时刻反应系统该物理量L的值,cA0,cA分别表示0,t时刻反应组分A的浓度值。)
第6题
利用分光光度法测定总氮的过程是:向水样中加入______进行消解(120℃加热分解30min,或120℃:以下紫外分解,或100℃以下氧化分解),氧化分解生成的______可用紫外分光光度计进行测量。
第7题
在67℃时,获得N2O5(g)分解反应
| t/s | 0.0 | 60.0 | 120.0 | 180.0 | 240.0 |
| c(N2O5)/(mol·L-1) | 0.160 | 0.113 | 0.080 | 0.056 | 0.040 |
第8题
在一定温度下,二硫化碳能被氧氧化,其反应方程式与标准平衡常数如下:
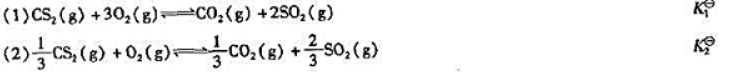
试确定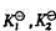 之间的数量关系.
之间的数量关系.
第9题
已知在1mol/L HCl介质中,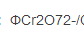 /Cr3+)=1.00V,
/Cr3+)=1.00V,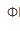 (Fe3+/Fe2+)=0.68V,以K7Cr2O7滴定Fe2+时,适宜的指示剂为( )。
(Fe3+/Fe2+)=0.68V,以K7Cr2O7滴定Fe2+时,适宜的指示剂为( )。
A.自身作指示剂 B.邻苯氨基苯甲酸(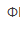 =0.89V)
=0.89V)
C.亚甲基蓝(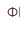 =0.52V)D.邻二氮菲亚铁(
=0.52V)D.邻二氮菲亚铁(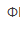 =1.06V)
=1.06V)
第10题
某温度下,N2O5按下式分解:
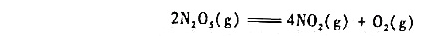
由实验测得在67℃时N2O5浓度随时间的变化如下:

试求:
(1)0-2min内的平均反应速率;
(2)t=2min时的瞬时反应速率。
第11题
已知PCl5的热分解反应:
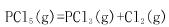
某温度时,在容积为10L的密闭容器中的2mol PCl5有1.5mol分解了,计算此温度时的平衡常数Kc。