 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
对于反应: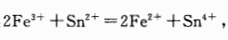 下列叙述正确的是()。
下列叙述正确的是()。
A.滴定曲线对称
B. 滴定曲线不对称,计量点的电势偏向 Sn4+ /Sn2+ 电对一方
C.滴定曲线不对称,计量点的电势偏向Fe3+ /Fe2+电对一方
D. 突跃大小与反应物的初始浓度有关
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
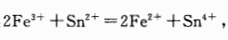 下列叙述正确的是()。
下列叙述正确的是()。A.滴定曲线对称
B. 滴定曲线不对称,计量点的电势偏向 Sn4+ /Sn2+ 电对一方
C.滴定曲线不对称,计量点的电势偏向Fe3+ /Fe2+电对一方
D. 突跃大小与反应物的初始浓度有关
 答案
答案
 更多“对于反应:下列叙述正确的是()。A. 滴定曲线对称B. 滴定曲线不对称,计量点的电势偏向 Sn4+ /Sn”相关的问题
更多“对于反应:下列叙述正确的是()。A. 滴定曲线对称B. 滴定曲线不对称,计量点的电势偏向 Sn4+ /Sn”相关的问题
第1题
试写出下列反应的化学方程式,并叙述实验现象:
(1)过量浓氨水与氯气反应。
(2)使砷化氢通过一玻璃管,并在玻璃管的入口处加热。
(3)向氯化钙溶液中加入磷酸氢钠溶液,充分反应后:
①滴加氨水:②滴加HAc。
(4)在三氯化铁溶液中逐滴加入磷酸钠,直至大过量。
(5)在三氯化锑溶液中逐滴加入氢氧化钠,直至大过量。
(6)将三氯化铋加到氢氧化钠溶液中,充分反应后,通入Cl2。
第2题
A.向淀粉溶液中加入碘—碘化钾溶液,反应后呈橙黄色
B.向葡萄糖溶液中加入本尼迪特试剂,加热后呈红黄色
C.向蛋清液中加入双缩脲试剂A液,加热后溶液呈紫色
D.用苏丹Ⅲ染液处理花生子叶切片,观察到油滴呈蓝色
第3题
试写出下列反应的化学方程式,并叙述实验现象:
(1)向CuSO4溶液中加入适量NaOH,将滤出的沉淀物微热,之后再加强热;
(2)试管中有适量无水硫酸铜,加水后充分振荡,之后加入过量碘化钾溶液,充分反应后再加入过量硫代硫酸钠;
(3)向硝酸汞溶液中滴加碘化钾至过量,用氢氧化钾调pH后,再加入适量氯化铵;
(4)向二价钒离子的溶液中逐滴加入高锰酸钾溶液直至过量;
(5)向Co2+溶液中加入戊醇后,再加入过量KSCN溶液;
(6)向用硫酸酸化的重铬酸钾溶液中滴加硫化氢溶液;
(7)向NiSO4溶液中加入过量NaOH,充分反应后滴加氯水。
第4题
A.盐酸与铁生锈反应后溶液呈浅绿色
B.硝酸铵在水中溶解时溶液温度降低
C.将紫外石蕊溶液滴入Na2CO3溶液中溶液变蓝
D.硫在氧气中燃烧发出蓝紫色火焰
第5题
A.滴定曲线对称
B. 滴定曲线不对称,计量点的电势偏向Sn4+/Sn2+电对一方
C. 滴定曲线不对称,计量点的电势偏向Fe3+/Fe2+电对一方
D. 突跃大小与反应物的初始浓度有关
第6题
A. 化学平衡状态是正逆反应都停止的状态
B. 对于可逆反应C(s)+ H20(g) = CO(g) + H2(g),在一定温度下达到平衡,ρ(H20)=ρ(CO)=ρ(H2) ,即反应物与生成物压力相等
C. 反应N2(g) +02(g) =2NO(g)和2N2(g) +202(g) =4NO(g)虽代表同一反应,但是它们的标准平衡常数不相等
D. 多步反应的总标准平衡常数为各步反应标准平衡常数之和
第7题
A.配制FeCl3(aq):称取一定质量的FeCl3(s),加水溶解,再加入稀盐酸酸化
B.钠与水的反应:取绿豆大小的金属钠放入烧杯,再滴入两滴酚酞试液,最后加入水
C.析出溶质晶体:接近饱和的热溶液,冷却速度越慢得到的晶体颗粒越大
D.实验室制氢气:为了加快反应速率,向稀H2SO4中滴加少量Cu(NO3)2
第8题
A.对于单相化学反应,在温度不变的条件下,任何瞬间的化学反应速度与该瞬间的参加反应的反应物浓度的幂次方的乘积成正比
B.化学反应速度可表示为
C.无论简单反应活着复杂反应,反应级数为反应式中各反应物浓度项的指数之和
D.化学反应速度常数的大小直接取决于反应温度及反应物的物理化学性质
第9题
由△Gθ-T图,讨论下列问题:
将Cu(N03)2缓慢滴人NH4HCO3溶液中(倒滴法),反应初期不见沉淀析出,为什么?随着Cu(NO3)2的不断加入发现有沉淀产生,试判断是何种沉淀。写出有关的离子反应方程式。
第10题
A.l2与H2O反应:Cl2+H2O = 2H++ClO-+ Cl-
B.向Na2SiO3溶液中逐滴加入稀盐酸:2H+ +SiO32- ═ H2SiO3(胶体)
C.向AlCl3溶液中滴加氨水至过量:Al3+ + 3OH- ══ Al(OH)3↓
D.将铜片投入稀盐酸中: Cu + 2H+ = Cu2+ + H2↑