 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
一个可逆电动势为1.07V的原电池,在恒温槽中恒温至293K,当此电池短路(即直接发生化学反应,不做电功)时有1000
一个可逆电动势为1.07V的原电池,在恒温槽中恒温至293K,当此电池短路(即直接发生化学反应,不做电功)时有1000C的电荷量通过。假定电池中发生的反应与可逆放电时的反应相同,试求以此电池和恒温槽都看做系统时总的熵变。如果要分别求算恒温槽和电池的熵变,还需何种数据?
 答案
答案

 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
一个可逆电动势为1.07V的原电池,在恒温槽中恒温至293K,当此电池短路(即直接发生化学反应,不做电功)时有1000C的电荷量通过。假定电池中发生的反应与可逆放电时的反应相同,试求以此电池和恒温槽都看做系统时总的熵变。如果要分别求算恒温槽和电池的熵变,还需何种数据?
 答案
答案

 更多“一个可逆电动势为1.07V的原电池,在恒温槽中恒温至293K,当此电池短路(即直接发生化学反应,不做电功)时有1000”相关的问题
更多“一个可逆电动势为1.07V的原电池,在恒温槽中恒温至293K,当此电池短路(即直接发生化学反应,不做电功)时有1000”相关的问题
第1题
第2题
计算原电池(一)Cu|Cu2+(1.0 mol·kg-1)||Ag+(1.0 mol·kg-1)|Ag()在下述情况下电动势改变值:(1)Cu2+浓度降到1.0X10-3mol·kg-1(2)加入足量的CI-使AgCl沉淀,设CI-浓度为1.561 mol·kg-1
第3题
将反应Ag(s)→Ag-Au(合金,a(Ag)=0.1)设计成原电池图式为______,25℃时该电池的电动势E=______。
第4题
A.0.1 mol.dm-3HCl
B.0.1 mol.dm-3HAe+0.1 mol.dm-3NaAc
C.0.1 mol.dm-3HAc
D.0.1 mol.dm-3H2PO4
第5题
原电池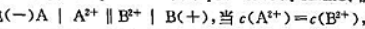 其电动势为0.360V,若c(A2+)=0.100mol·L-1,c(B2+)=1.00X10-4mol·L-1,此时电池电动势是多少?
其电动势为0.360V,若c(A2+)=0.100mol·L-1,c(B2+)=1.00X10-4mol·L-1,此时电池电动势是多少?
第7题
在由铜片和CuSO4溶液、银片和AgNO3溶液组成的原电池中,如将CuSO4溶液加水稀释,原电池的电动势会减少。( )
第8题
(1)写出下列各电对的电极反应式,并根据元素电势图给出各电极反应的标准电极电势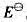 。
。
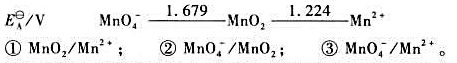
(2)试写出以电对①为负极、电对②为正极的原电池的电池反应,并计算原电池的标准电动势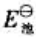 和电池反应的
和电池反应的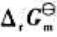 。
。
(3)试写出以电对①为负极、电对③为正极的原电池的电池反应,并计算原电池的标准电动势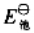 和电池反应的
和电池反应的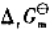 。
。
第9题
第10题
A.增加
B.减少
C.不变
D.无法判断
第11题
已知

Cd|Cd2+(0.10mol·L-1)||Sn4+(0.10mol·L-1),Sn2+(0.0010mol·L-1)|Pt在298K时的电动势ε,并写出电池反应,标明正、负极。