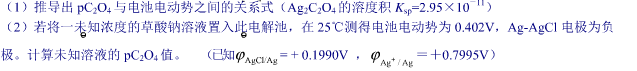题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
298K时,AgCl在水中的饱和浓度为1.27×10-5mol·kg-1,根据Debye-Huckel理论计算反应AgCl====Ag+(aq)+Cl-(aq)的
298K时,AgCl在水中的饱和浓度为1.27×10-5mol·kg-1,根据Debye-Huckel理论计算反应AgCl====Ag+(aq)+Cl-(aq)的标准Gibbs自由能
 答案
答案
在水溶液中,AgCl的离子强度为

则AgCl的平均离子活度因子为
γ±=0.9958
故题给反应的标准Gibbs自由能为
=-[2×8.3145×298×ln(0.9958×1.27×10-5)]J·mol-1
=55.9kJ·mol-1
在KNO3溶液中,AgCl的平均离子活度因子为
γ±=0.8894
则AgCl在KNO3溶液中的饱和浓度为





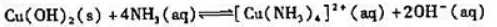
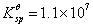 ,AgCl的
,AgCl的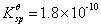 。
。