 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
已知下列电对的标准电极电势:在酸性溶液中分别用1.0mol·L-1Fe2+,1.0mol·L-1
已知下列电对的标准电极电势:
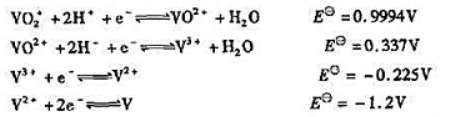
在酸性溶液中分别用1.0mol·L-1Fe2+,1.0mol·L-1Sn2+和Zn还原1.0mol·L-1的VO2+时,最终得到的产物各是什么(不必计算)?
 答案
答案
查看答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知下列电对的标准电极电势:
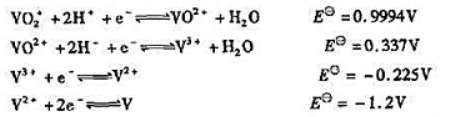
在酸性溶液中分别用1.0mol·L-1Fe2+,1.0mol·L-1Sn2+和Zn还原1.0mol·L-1的VO2+时,最终得到的产物各是什么(不必计算)?
 答案
答案
 更多“已知下列电对的标准电极电势:在酸性溶液中分别用1.0mol·L-1Fe2+,1.0mol·L-1”相关的问题
更多“已知下列电对的标准电极电势:在酸性溶液中分别用1.0mol·L-1Fe2+,1.0mol·L-1”相关的问题
第1题
第3题


已知c(
第4题

 ,试计算在c(H+)=1.0mol/L,c(
,试计算在c(H+)=1.0mol/L,c(


第6题
第7题
电极反应: ,计算电对
,计算电对



第8题
对于电对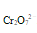 /Cr3+,溶液pH上升,则其( )。
/Cr3+,溶液pH上升,则其( )。
A.电极电势下降 B.电极电势上升
C.电极电势不变 D.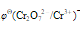 下降
下降
第9题
计算Cu2+的浓度为0.001mol·L-1时,电对Cu2+/Cu的电极电势。已知
第11题
已知下列电极反应的标准电极电势:
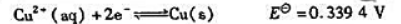
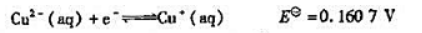
(1)计算反应: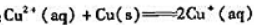 的KΘ;
的KΘ;
(2)已知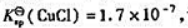 计算反应:
计算反应:
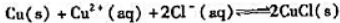 的标准平衡常数KΘ:
的标准平衡常数KΘ: