 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
查出下列电对的标准电极电势,分别指出各组中最强的氧化剂和最强的还原剂。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
 更多“查出下列电对的标准电极电势,分别指出各组中最强的氧化剂和最强的还原剂。”相关的问题
更多“查出下列电对的标准电极电势,分别指出各组中最强的氧化剂和最强的还原剂。”相关的问题
第1题
(1)试写出下列各电对的电极反应式:
①H+/H2;②O2/H2O;③OH-/H2:④O2/OH-
(2)查表求出①和④的标准电极电势值,并分别写出其电极电势的能斯特方程。
(3)试根据①和④的标准电极电势值及水的离子积常数,求出②和③的标准电极电势值。
第2题
Fe3+可以作为H2O2歧化(分解)反应的催化剂.若该反应的机理为
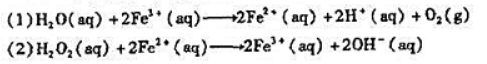
总反应:2H2O2(aq)→2H2O(l)+O2(g)
查出相关电对的标准电极电势,说明上述机理的可行性.并推断Ca2+催化H2O2分解的反应机理.
第4题
已知下列电对的标准电极电势:
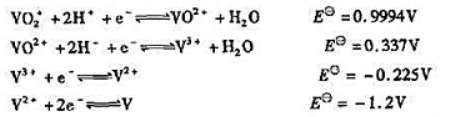
在酸性溶液中分别用1.0mol·L-1Fe2+,1.0mol·L-1Sn2+和Zn还原1.0mol·L-1的VO2+时,最终得到的产物各是什么(不必计算)?
第6题
A.
B.同一元素有多种氧化态时,不同氧化态组成的电对的
C.电对中有气态物质时,
D.由同一金属不同氧化态的离子组的氧化还原电极,当氧化态和还原态浓度相等时的电极电势就是标准电极电势
第7题
(1)写出下列各电对的电极反应式,并根据元素电势图给出各电极反应的标准电极电势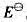 。
。
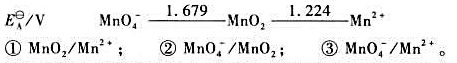
(2)试写出以电对①为负极、电对②为正极的原电池的电池反应,并计算原电池的标准电动势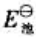 和电池反应的
和电池反应的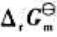 。
。
(3)试写出以电对①为负极、电对③为正极的原电池的电池反应,并计算原电池的标准电动势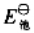 和电池反应的
和电池反应的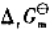 。
。
第8题
A.E1-E2
B.E1-2E2
C.E2-E1
D.2E2-E1
第9题
A.Fe2+/Fe电对的标准电极电势下降
B.Fe2+/Fe电对的标准电极电势上升
C.H+/H2电对的电极电势因(H+)上升而上升
D.H+/H2电对的标准电极电势上升
第10题