 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在298K和标准压力时,电解一含Zn2+溶液,希望当Zn2+浓度降至1×10-4mol·kg-1时,仍不会有H2(g)析出,试问溶液的p
在298K和标准压力时,电解一含Zn2+溶液,希望当Zn2+浓度降至1×10-4mol·kg-1时,仍不会有H2(g)析出,试问溶液的pH值应控制在多少为好?已知H2(g)在Zn(s)上的超电势为0.72V,并设此值与溶液浓度无关。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在298K和标准压力时,电解一含Zn2+溶液,希望当Zn2+浓度降至1×10-4mol·kg-1时,仍不会有H2(g)析出,试问溶液的pH值应控制在多少为好?已知H2(g)在Zn(s)上的超电势为0.72V,并设此值与溶液浓度无关。
 答案
答案
 更多“在298K和标准压力时,电解一含Zn2+溶液,希望当Zn2+浓度降至1×10-4mol·kg-1时,仍不会有H2(g)析出,试问溶液的p”相关的问题
更多“在298K和标准压力时,电解一含Zn2+溶液,希望当Zn2+浓度降至1×10-4mol·kg-1时,仍不会有H2(g)析出,试问溶液的p”相关的问题
第1题
已知298K,CO2的分压为101325Pa时,与之平衡的1dm3的水能溶解0.8266dm。的CO2,设溶于水中的CO2全部生成H2CO3,并且H2CO3在水中仅发生一级解离,其标准解离平衡常数为4.7×10-7,活度因子均为1。假定水的电导率仅由H-和

第2题
根据下列在298K和标准压力下的热力学数据,计算HgO(s)在该温度时的解离压。
(1)电池Pt|H2(PH2) |NaOH(a) |HgO(s) |Hg(I)的标准电动势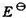 =0.9265V;
=0.9265V;
(2)反应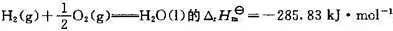 ;
;
(3)298K时,下表为各物质的标准摩尔熵值:

第3题
第4题
A.理想气体从1×107Pa反抗恒定的压力1×105Pa膨胀到1×105Pa
B.0℃、101325Pa下冰融化成水
C.101325Pa下电解CuSO4水溶液
D.气体从298K、101325Pa可逆变化到373K、10132.5Pa
第5题
电解1.000×10-2mol·L-1硫酸锌溶液,当介质为0.50mol·L-1硫酸溶液时,锌是否能在铂电极上析出?如果介质[H<sup>+</sup>]=10-5mol·L-1时,锌是否能析出?(在锌电极上,ηH2=-0.70V;E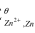 (zn2+/zn)=-0.763V)
(zn2+/zn)=-0.763V)
第7题
第8题
在锌电极上析出氢气的Tafel公式为
η/V=0.72+0.116lg[j/(A·cm-2)]
在298K时,用Zn(s)作阴极,惰性物质作阳极,电解浓度为0.1mol·kg-1的ZnSO4溶液,设溶液pH值为7.0,若要使H2(g)不和锌同时析出,应控制什么条件?
第9题
图是三组分系统KNO3-NaNO3-H2O的相图,实线是298K时的相图,虚线是373K下的相图。一机械混合物含70%的KNO3及30%的NaNO3,清根据相图拟定分离步骤。
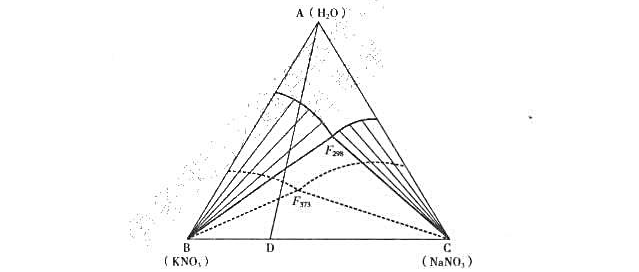
第10题
在298K时,某溶液含MgCl2和ZnSO4的浓度均为0.002mol·kg-1,试用Debye-Htickel极限公式求ZnSO4的离子平均活度因子。
第11题
Ag2O遇热分解:2Ag2O(s)=4Ag(s)+O2(g),已知在298K时,Ag2O(s)的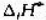 =-30.6kJ·mol-1,
=-30.6kJ·mol-1,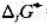 =-11.2kJ·mol-1,试求在298K时
=-11.2kJ·mol-1,试求在298K时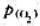 的压力是多少(Pa)?Ag2O(s)的热分解温度是多少?(105Pa下)
的压力是多少(Pa)?Ag2O(s)的热分解温度是多少?(105Pa下)